近日,核医学科陈皓鋆教授团队在医学影像领域顶级期刊 《Journal of Nuclear Medicine》发表了题目为“Fibroblast Activation Protein–Targeted PET/CT with 18F-Fibroblast Activation Protein Inhibitor-74 for Evaluation of Gastrointestinal Cancer: Comparison with 18F-FDG PET/CT”(doi:10.2967/jnumed.123.266329)的临床研究。在这篇文章中,作者报告了18F标记FAP放射性探针18F-FAPI-74在消化道肿瘤(包括胃癌、肝癌、胰腺癌)中的PET/CT显像应用,并与常规18F-脱氧葡萄糖(FDG)进行了比较。本文的通讯作者为厦门大学附属第一医院核医学科的陈皓鋆教授。厦门大学附属第一医院硕士生徐伟植、蔡佳宇、厦门大学附属第一医院核医学科高级工程师彭添兴共同第一作者。

原文链接:
https://jnm.snmjournals.org/content/early/2023/10/26/jnumed.123.266329.long
研究背景介绍
超过90%的恶性上皮组织肿瘤的癌相关成纤维细胞(CAFs)高表达成纤维细胞激活蛋白(FAP),其中在胃癌和胰腺癌中的阳性表达率均超过50%。FAP是表达于CAF上的Ⅱ型膜结合糖蛋白,具有二肽基肽酶和内肽酶活性。FAP抑制剂 (FAPI)可以特异性地与FAP结合。之前的研究表明,68Ga-FAPI在各种癌症中的诊断效能优于18F-FDG。然而,68Ga在临床应用中存在一些不足。首先,生产68Ga需要68Ge/68Ga发生器,每次洗脱只能满足少数几例患者的检查需求,限制了大规模使用。此外,68Ga半衰期较短(68分钟),限制了无68Ge/68Ga发生器的检查中心及偏远山区的使用。最后,68Ga的正电子能量较高,组织中的平均自由程较大,导致PET图像空间分辨率低。而18F可以由回旋加速器生产,并且具有中等半衰期(110分钟),且具有更高的正电子衰变率和更低的正电子范围,这些优势解决了68Ga的限制,且能满足远距离配送的要求。因此,18F是PET成像的理想核素。而随着医用回旋加速器的普及,18F可能更适合推广这种成像方式,使新型核医学显像剂惠及更多患者。18F-FAPI-74(LNC1005)是一种由正电子核素18F标记的FAP靶向PET示踪剂,已成功用于各种癌症患者的成像。然而,18F-FAPI-74 PET/CT在胃肠道肿瘤中的临床研究报告相对较少。前期68Ga-FAPI的PET显像结果鼓励我们进一步探索18F-FAPI-74 PET/CT在消化道肿瘤中的临床应用。
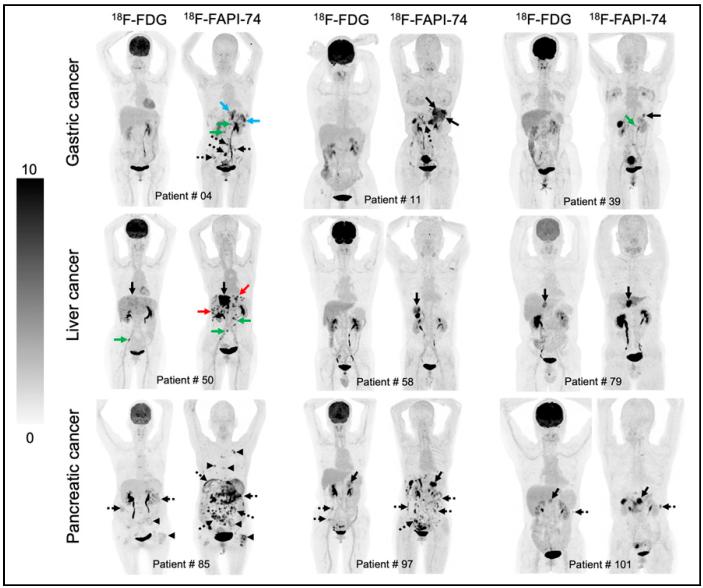
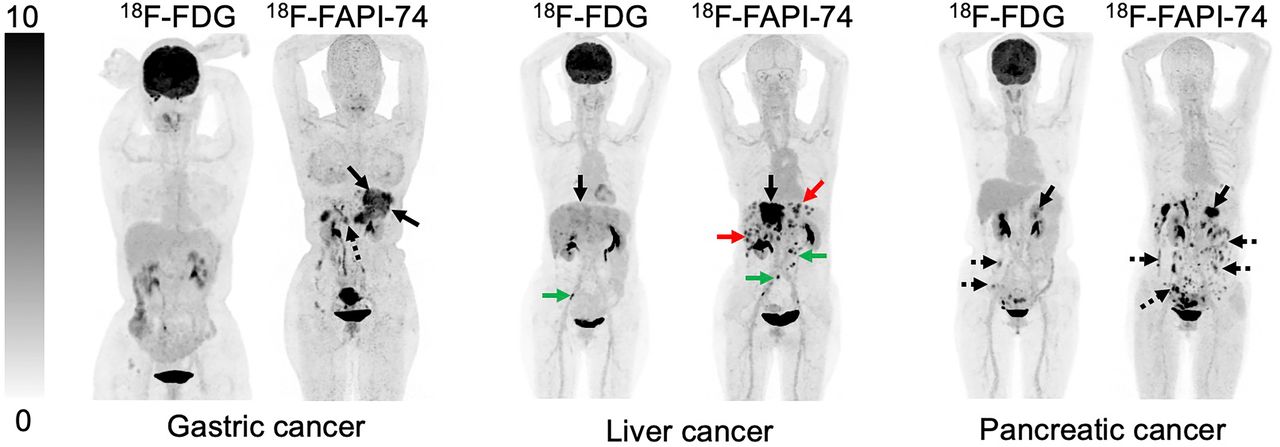
18F-FAPI-74和18F-FDG PET/CT在消化系统肿瘤中的成像对比
研究方法
研究对象
这项研究是在厦门大学附属第一医院核医学科进行的一项单中心、前瞻性临床研究,旨在评估18F-FAPI-74 PET/CT在诊断消化系统肿瘤(包括胃癌、肝细胞癌、胆管癌、和胰腺癌)中的诊断效能,并将其结果与18F-FDG PET/CT进行比较。在这项研究中,研究团队在2022年6月至2022年12月期间共纳入112例消化系统肿瘤患者。纳入标准如下:在治疗前已被确诊或怀疑胃癌、肝癌和胰腺癌的患者;治疗后,因临床实验室检查(如肿瘤标志物)或诊断影像(如CT、MRI或超声)怀疑复发或转移的患者。患者同意接受18F-FDG和18F-FAPI-74 PET/CT的检查,两个扫描之间的时间间隔小于1周。排除标准包括:非恶性病变或经病理证实非消化系统肿瘤的患者;在PET显像前4周接受其他抗肿瘤治疗的患者;以及无法或不愿提供书面知情同意的研究参与者、父母或法定代表人。
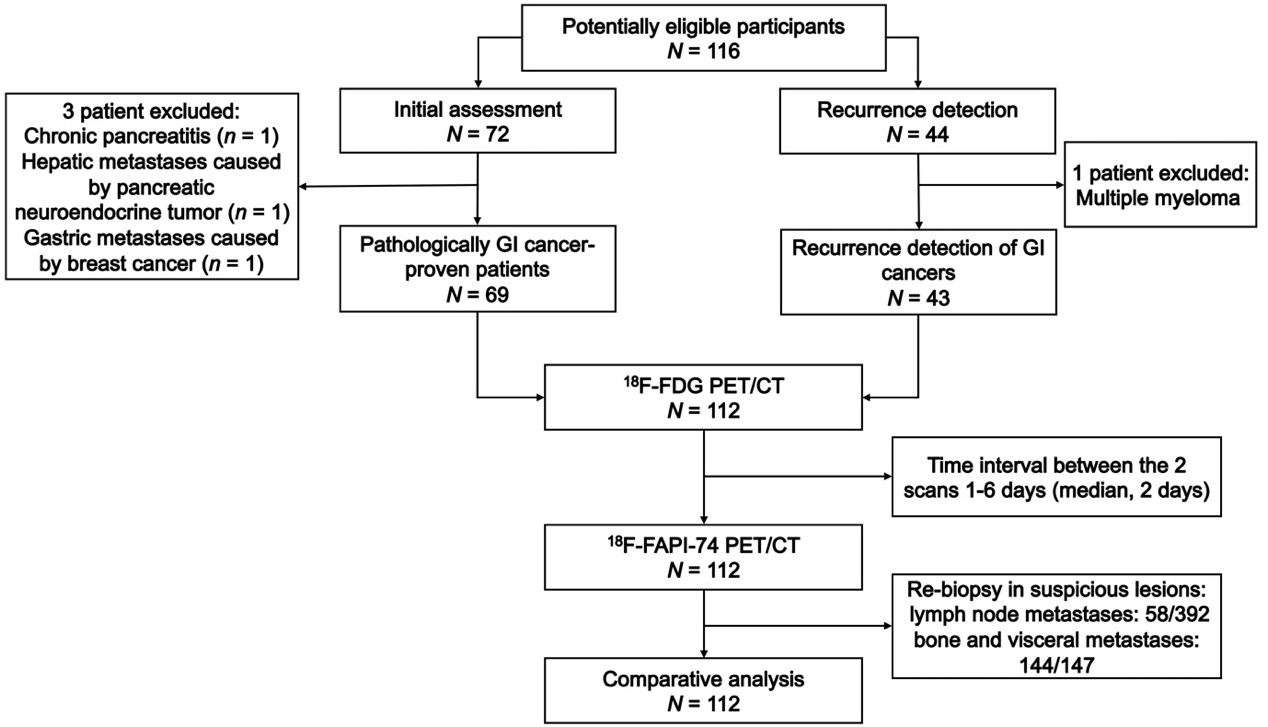
图1. 临床研究流程图
显像剂制备
依照前期文献报告(Giesel FL, Adeberg S, Syed M, et al. JNucl Med. 2021;62:201–207)所述方法进行18F-FAPI-74(18F-LNC1005)显像剂的制备。18F-FDG(18氟-2-脱氧葡萄糖)由本实验室使用Traceer lab FXFC合成模块(美国GE公司)合成。18F-FDG和18F-FAPI-74的放射化学纯度均超过95%,用生理盐水稀释,并通过0.22 μm Millex过滤器(美国Millipore公司)过滤到无菌注射器中进行灭菌,最终产物均符合无菌标准和人体给药注射标准。
PET/CT显像流程及图像分析
对于18F-FDG PET/CT,患者禁食6小时以上,并在注射18F-FDG (5.55 MBq/kg)之前监测血糖水平,在注射63.0+4.9分钟(范围,50 - 75分钟)后进行PET/CT成像。18F-FAPI-74的注射剂量为210.9+48.1 MBq (注射范围129.5-333 MBq),经注射后63.3+4.0分钟 (范围,50 - 80分钟)进行PET/CT成像(每个床位1.5 min),扫描使用CT参数如下:管电压110keV,管电流110mA, 层厚3.75mm。CT扫描后立即行PET扫描,每个床位采集时间为1.5 min,采集6-8个床位,PET扫描采用3D静态模式。使用CT重建数据对PET图像进行衰减校正。数据重建使用贝叶斯正则化似然重建算法(Bayesian penalized likelihood, BPL)。18F-FDG和18F-FAPI-74 PET/CT的图像判读分析分2组进行,每组均由2位经验丰富的核医学医师进行独立阅片。意见不统一时经共同讨论后达成一致。以患者的手术/穿刺病理结果作为最终诊断的金标准。对无法获得手术/穿刺病理结果的可疑病灶,以实验室检查、临床及影像随访结果作为最终诊断的参考标准。
统计学分析
使用IBM SPSS 26.0软件进行统计分析。为了评估18F-FAPI-74和18F-FDG PET/CT的诊断性能,用McNemar检验比较18F-FAPI-74和18F-FDG PET/CT显示的阳性病灶数,用Wilcoxon符号秩检验评估两种PET/CT显像间SUVmax和TBR的差异。采用McNemar检验评估18F-FAPI-74和18F-FDG PET/CT诊断的准确性。P<0.05为差异有统计学意义。
数据分析
根据纳排标准,本研究共纳入112例消化系统患者(男性76例,女性36例),具体包括:49例胃癌(男性31/49;中位年龄,62岁),39例肝癌患者(31/39男性;平均年龄62岁),24例胰腺癌(14/24男性;在112例患者中,69例(62%)接受PET/CT检查以进行肿瘤的初始分期,43例(38%)患者接受PET/CT检查进行肿瘤的复发/转移监测(再分期)。18F-FDG和18F-FAPI-74 PET/CT两次检查间的时间间隔为2天(范围1-6天)。患者的临床特征见表1。
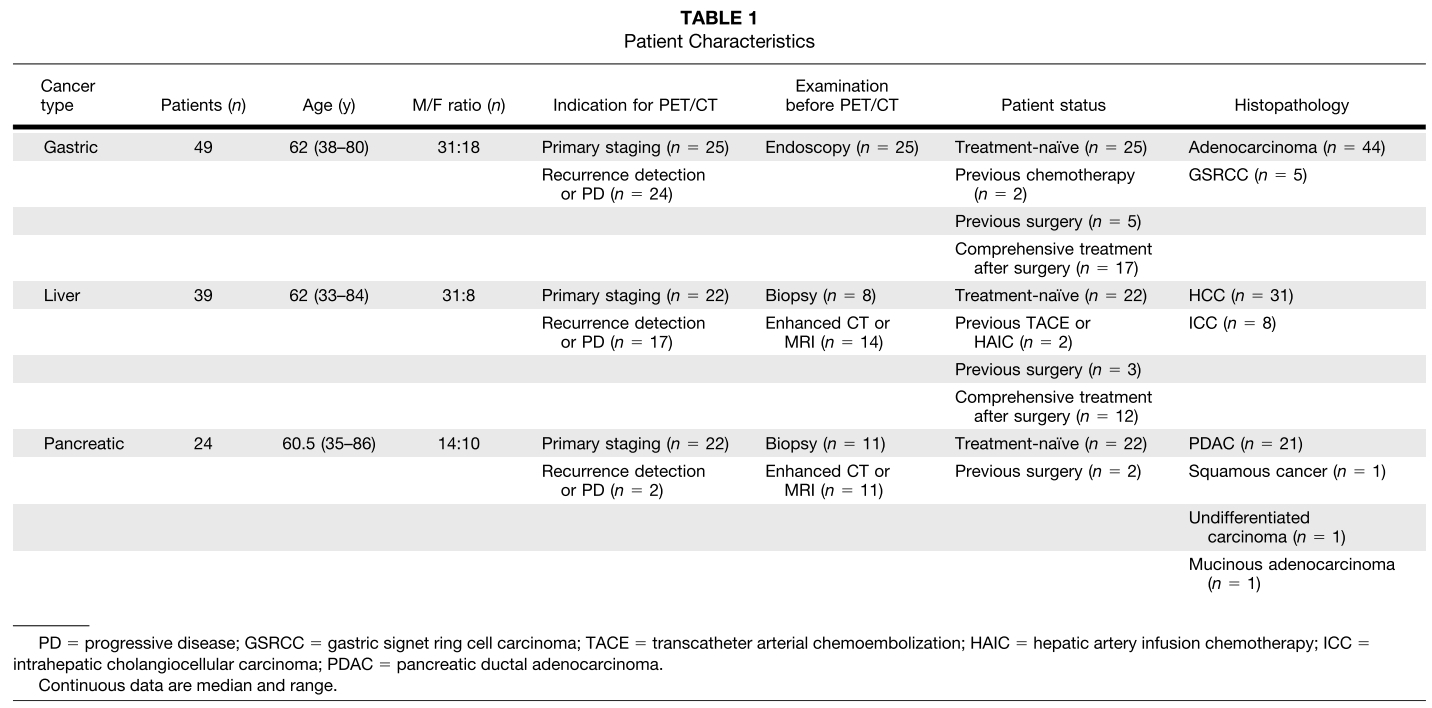
表1.患者临床特征
18F-FAPI-74与18F-FDG PET/CT在胃癌中的成像对比
49例胃癌患者中,病理类型为腺癌的共44例,印戒细胞癌共5例。与18F-FDG PET/CT相比,18F-FAPI-74 PET/CT显示的转移淋巴结数量更多(88% [104/118] vs. 55% [65/118]; P<0.001),示踪剂摄取更高(中位SUVmax,6.2 vs. 2.9; P<0.001),并且腹部淋巴结靶/本底比 (TBR) (中位数,4.5 vs. 1.7;P<0.001)和膈上区淋巴结的TBR (中位数,4.4 vs. 2.6;P = 0.010)在18F-FAPI-74 PET/CT中更高。对于骨和内脏转移,18F-FAPI-74 PET/CT显示的腹膜转移病灶数量显著多于18F-FDG (100% [145/145] vs 64% [38/145]; P<0.001),且18F-FAPI-74的示踪剂摄取(中位SUVmax,6.9 vs. 2.5; P<0.001)及TBR(中位数,5.8 vs 1.4; P<0.001)较18F-FDG更高。此外,与18F-FDG相比,18F-FAPI-74 PET/CT在吻合口局部复发灶和骨转移病灶的诊断灵敏度及显像剂摄取程度方面,两者较为相似。图2展示了18F-FAPI-74在胃癌中优于18F-FDG的典型案例。
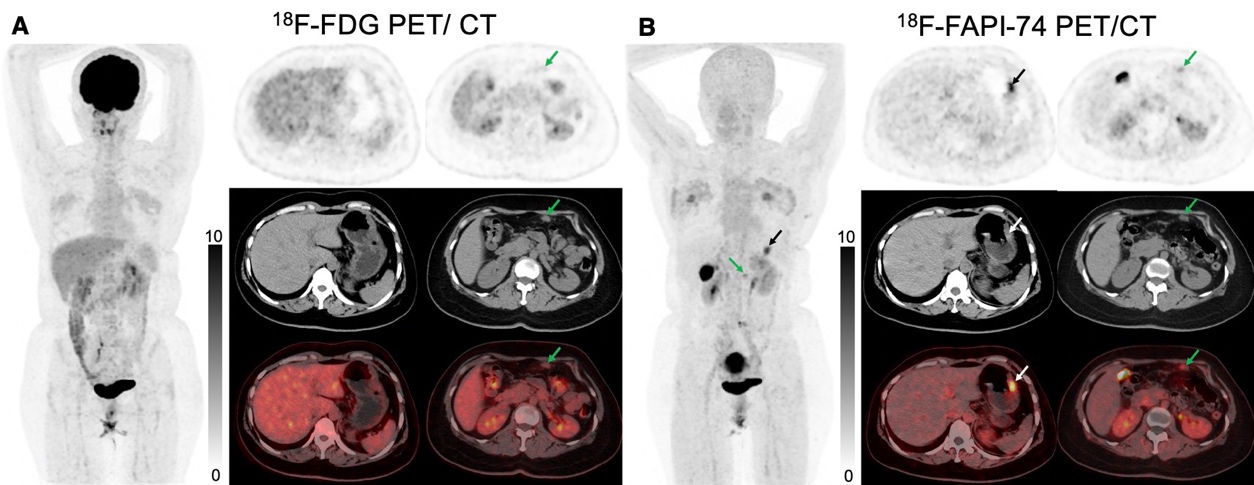
图2. 胃癌PET/CT的代表性病例(FAPI优于FDG)
图2. (A) 38岁女性,病理证实为胃印戒细胞癌,采用18F-FDG PET/CT进行初始分期,CT显示肠周稍大淋巴结,但18F-FDG低摄取 (箭头)。(B) 18F-FAPI-74 PET/CT显示原发病灶(黑色和白色箭头)和肠周淋巴结(绿色箭头)均呈现出明显的放射性摄取。随后经穿刺活检证实淋巴结为胃癌转移淋巴结 (右肾上方高摄取灶为胆囊生理性摄取)。
18F-FAPI-74与18F-FDG PET/CT在肝癌中的成像对比
39例肝癌患者中,病理类型为肝细胞肝癌(HCC)占31例,肝内胆管细胞癌(ICC)占8例。18F-FAPI-74 PET/CT显示出了所有的22例肝内原发肿瘤,诊断灵敏度为100% (22/22),而18F-FDG PET/CT漏诊4例(18/22, 82%)。在肝内转移灶的诊断方面,18F-FAPI-74 PET/CT优于18F-FDG (90% [46/51] vs. 53% [27/51]; P<0.001),在腹膜转移(100% [8/8] vs. 25% [2/8]; P = 0.031),术区局部复发灶 (92% [12/13] vs. 38% [5/13]; P = 0.016)和淋巴结转移灶 (97% [36/37] vs. 43% [16/37]; P<0.001)的诊断灵敏度方面,18F-FAPI-74也表现出显著的诊断优势,大部分病灶示踪剂摄取和TBR显著高于18F-FDG。肝癌的代表性PET/CT病例请参见图3。有意思的是,本研究的两例肝细胞癌患者中,18F-FDG显示更多数目的转移病灶(图4)。在这两例患者中,18F-FAPI-74 PET/CT显示出的13个阳性病灶(4个淋巴结转移和9个肝内转移),其摄取程度低于18F-FDG。
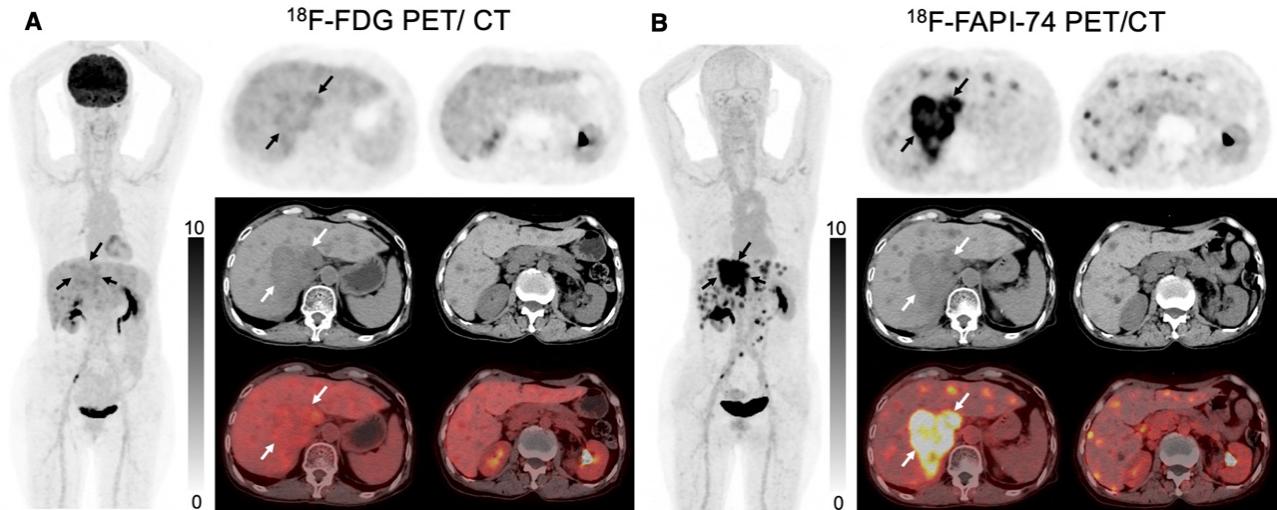
图3. 肝癌代表性病例(FAPI优于FDG)
图3. (A) 69岁女性,病理证实为肝内胆管细胞癌,PET/CT进行治疗前初始分期,显示原发肿瘤18F-FDG放射性轻度浓聚 (箭头)。(B) 18F-FAPI-74 PET/CT显示原发病灶中示踪剂强烈摄取 (箭头),并显示出更多数目的肝内转移灶。
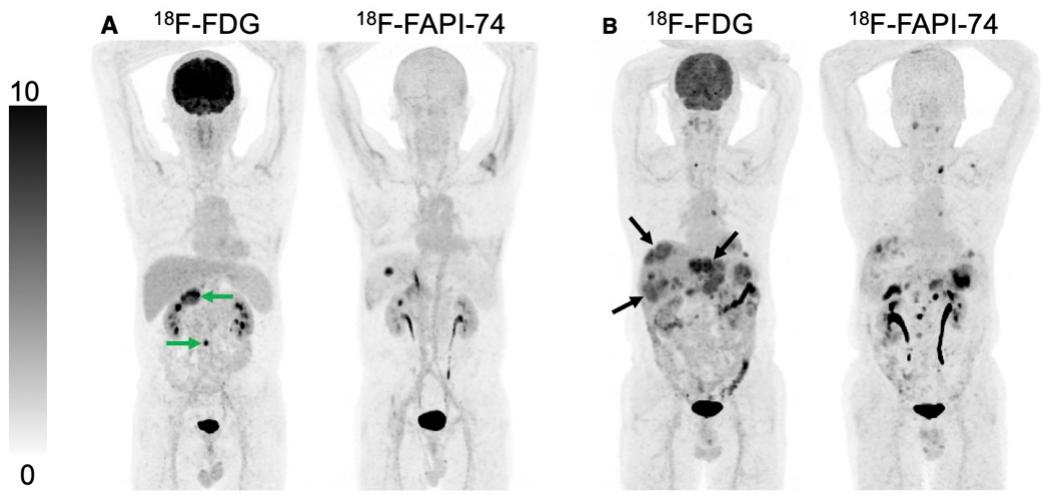
图4. 肝细胞癌PET/CT病例(FDG优于FAPI)
(A) 46岁男性接受18F-FDG PET/CT检测复发,随后活检证实腹部淋巴结转移。显示腹腔淋巴结转移的高放射示踪剂摄取(箭头)。18F-FAPI-74 PET/CT显示较低的放射示踪剂摄取和较少的腹腔淋巴结转移。肝脏的局灶性高代谢灶表明胆囊的生理性摄取。(B) 62岁,病理证实的肝癌患者行18F-FDG PET/CT首次分期,与18F-FAPI-74 PET/CT相比,18F-FDG PET/CT显示更多的肝内转移,摄取更高(箭头)
18F-FAPI-74与18F-FDG PET/CT在胰腺癌中的成像对比
胰腺癌共24例,其中病理为导管腺癌的占21例,腺鳞癌占1例,粘液腺癌占1例,未分化癌占1例。在原发肿瘤中,18F-FAPI-74 PET/CT和18F-FDG PET/CT的阳性率分别为22例和19例。原发肿瘤中的18F-FAPI-74摄取较18F-FDG更高(中位SUVmax, 16.5 vs. 7.3)。18F-FAPI-74 PET/CT比18F-FDG PET/CT显示更多转移灶,尤其是肝转移(100% [51/51] vs. 55% [28/51]; P<0.001)和腹膜转移(100% [41/41] vs. 44% [18/41]; P<0.001)。此外,18F-FAPI-74 PET/CT在淋巴结检出率(97% [36/37] vs. 41% [15/37]; P<0.001)、腹部区域淋巴结SUVmax (中位SUVmax, 9.6 vs. 2.5; P<0.001)和膈上区淋巴结SUVmax(中位SUVmax, 11.6 vs. 3.8; P=0.028)方面表现出更高的放射示踪剂摄取。在半定量分析中,18F-FAPI-74组的原发肿瘤SUVmax (中位SUVmax, 16.5 vs. 7.3; P<0.001),肝转移SUVmax (中位SUVmax, 7.5 vs. 4.0; P<0.001),腹膜转移SUVmax (中位SUVmax, 8.2 vs. 2.8; P<0.001)和骨转移SUVmax (中位SUVmax, 5.3 vs. 3.1; P=0.009) 均高于18F-FDG组。胰腺癌的典型病例请见图5。
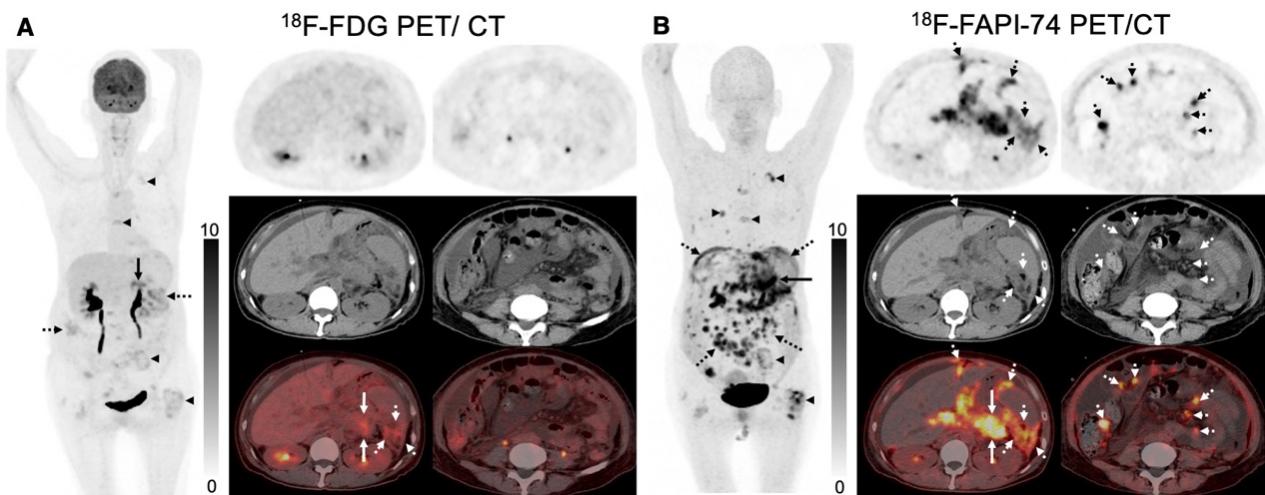
图5. 胰腺癌代表性病例(FAPI优于FDG)
(A) 55岁女性,活检证实为转移性骨肿瘤(原发灶不明),行18F-FDG PET/CT定位原发肿瘤; 18F-FDG PET/CT显示原发病灶(实线箭头)、腹膜转移灶(虚线箭头)和骨转移灶(箭头)呈低度摄取。(B) 18F-FAPI-74 PET/CT显示以上病灶的显像剂摄取显著高于18F-FDG,且18F-FAPI-74 PET/CT比18F-FDG显示出更大范围的腹膜转移灶。
18F-FAPI-74和18F-FDG PET/CT对消化系统肿瘤的诊断效能分析
69名初诊分期患者中,所有原发肿瘤均经组织活检(n = 57)及手术(n = 12)确认。与18F-FDG PET/CT对比,18F-FAPI-74 PET/CT对原发肿瘤的诊断具有更高的灵敏度(96% [66/69] vs. 75% [52/69]; P < 0.001),尤其是在胃癌的诊断,优势更为显著(88% [22/25] vs. 60% [15/25]; P = 0.016)。由于纳入标准限制(均为病理确诊的肿瘤患者),无法获取原发肿瘤的假阳性PET数据。因此,不能评估18F-FAPI-74和18F-FDG PET/CT对原发肿瘤诊断的特异性。通过影像随访、活检或手术的方式,对另外43例患者进行了局部复发/转移病灶的诊断效能评估。结果显示,18F-FAPI-74 PET/CT在局部复发病灶的诊断方面具有更高的灵敏度和准确性。在14名患者中,共392个淋巴结经手术病理确诊为肿瘤转移淋巴结。18F-FAPI-74 PET/CT对转移淋巴结的诊断较18F-FDG PET/CT具有更高的灵敏度和准确性。在89名患者中,共432个病灶经影像随访或手术/活检方式判定为转移性病变。18F-FAPI-74 PET/CT对骨及内脏转移的诊断方面较18FDG PET/CT具有更高的灵敏度,尤其对于腹膜种植转移及肝内转移的检测,18F-FAPI-74 PET/CT优势显著。
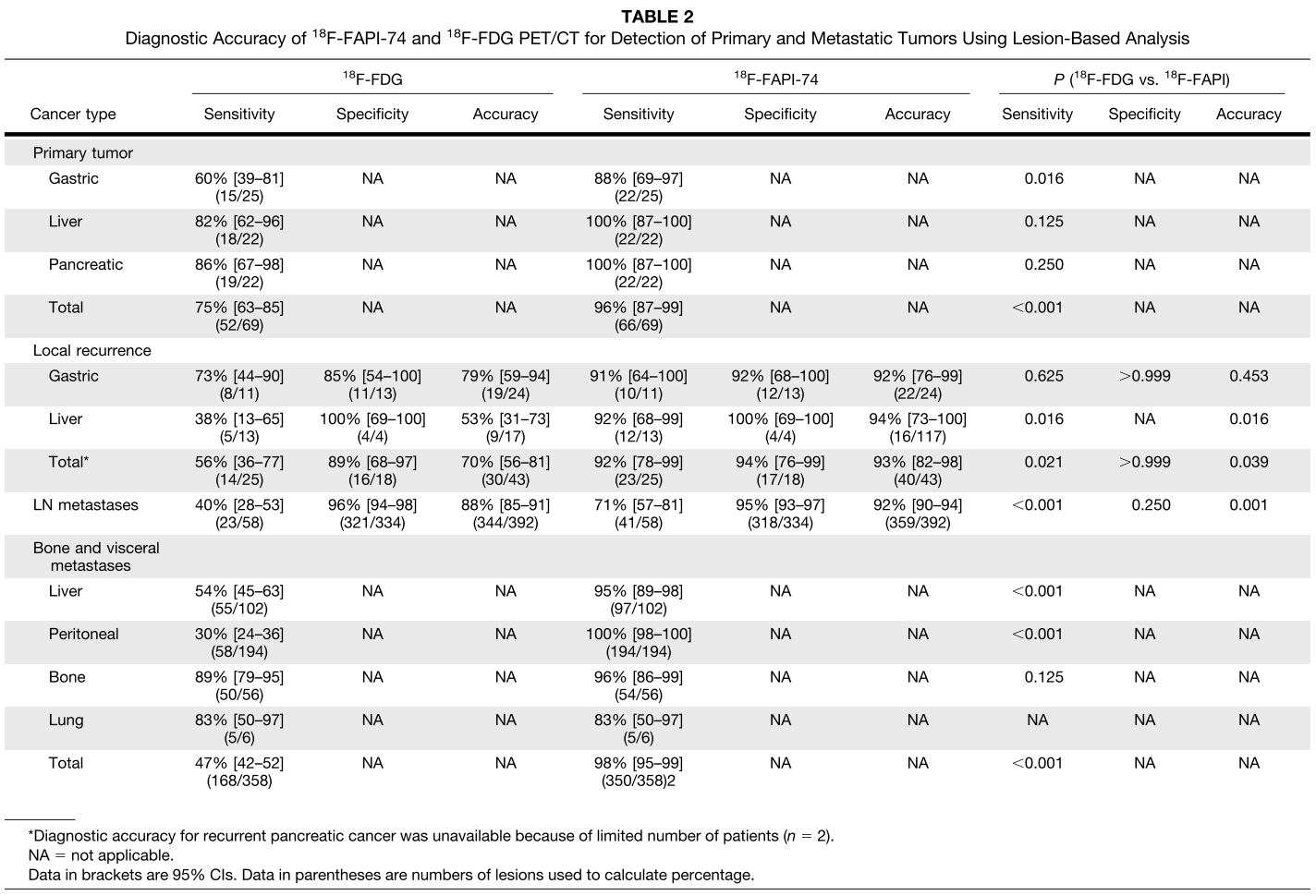
表2. 18F-FAPI-74和18F-FDG PET/CT的诊断效能分析(lesion-based)
18F-FAPI-74 PET/CT对TNM分期及临床治疗决策的影响
在69例初始分期患者中,18F-FAPI-74 PET/CT对17例患者(25%,17/69)判定的临床TNM分期高于经18F-FDG PET/CT判定的TNM分期(包括7例胃癌、6例肝癌和4例胰腺癌)。在69例初始分期患者中,有10例患者的原发肿瘤在18F-FAPI-74 PET/CT中可检出,而在18F-FDG PET/CT中被漏诊。另外,9例患者在18F-FAPI-74 PET/CT中显示出更大范围的腹膜转移灶,更多数目的淋巴结及内脏转移灶(详见表3)。43例存在复发或转移的患者中,18F-FDG PET/CT和18F-FAPI-74 PET/CT的真阳性率分别为56%(14/25)和92%(23/25)。此外,43例复发/转移患者中,有4例经病理确诊为局部复发(局部复发灶在18F-FAPI-74 PET/CT中可见,但18F-FDG PET/CT漏诊),18例显示出更大范围的腹膜转移病灶,14例显示更多数目的淋巴结、内脏和骨转移灶。基于以上结果,18F-FAPI-74 PET/CT改变了4例进展期消化道肿瘤患者的后续临床治疗决策(占总数的9%,4/43;见表4)。
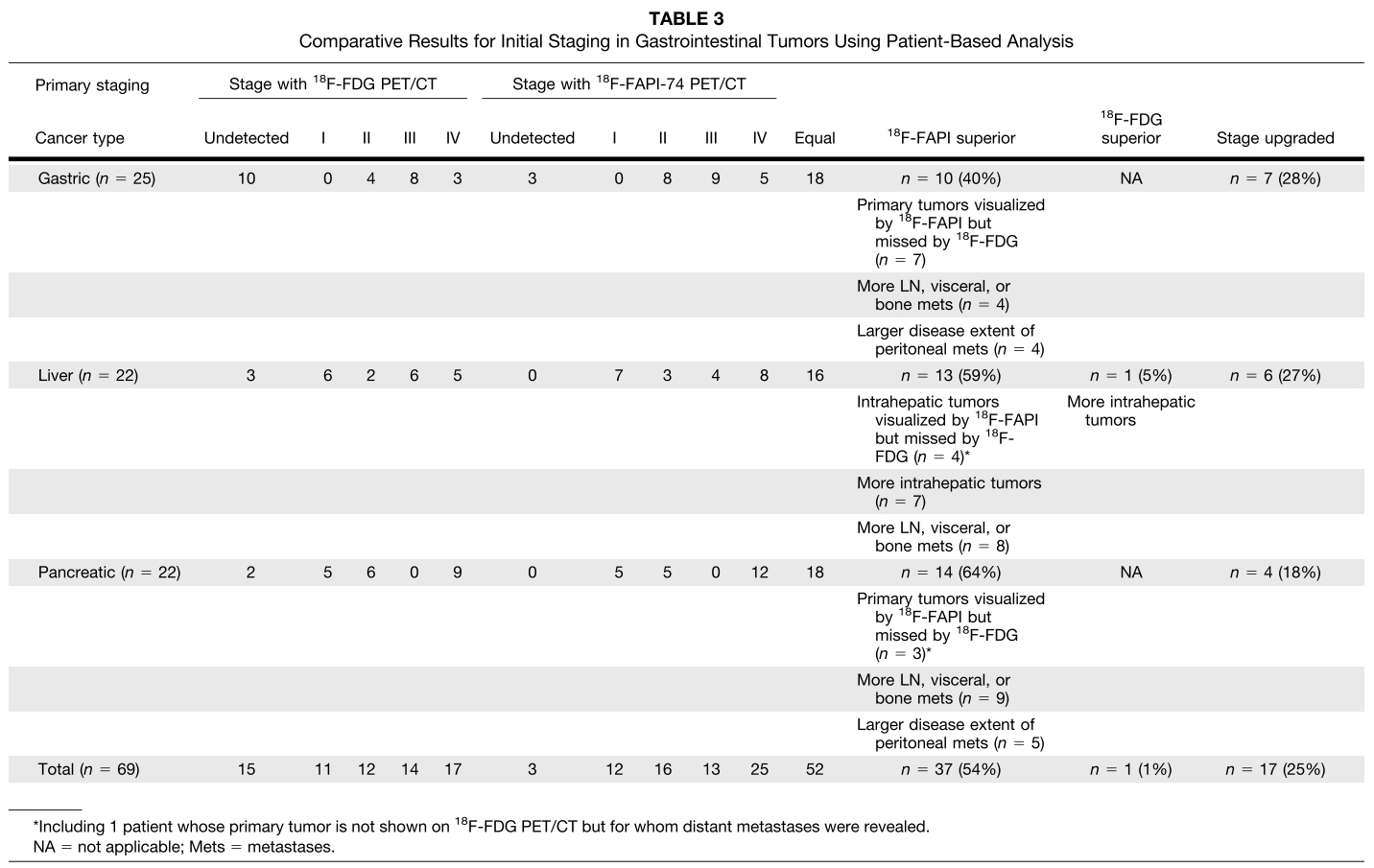
表3. 消化系统肿瘤初始分期的PET/CT对比结果(初诊患者)
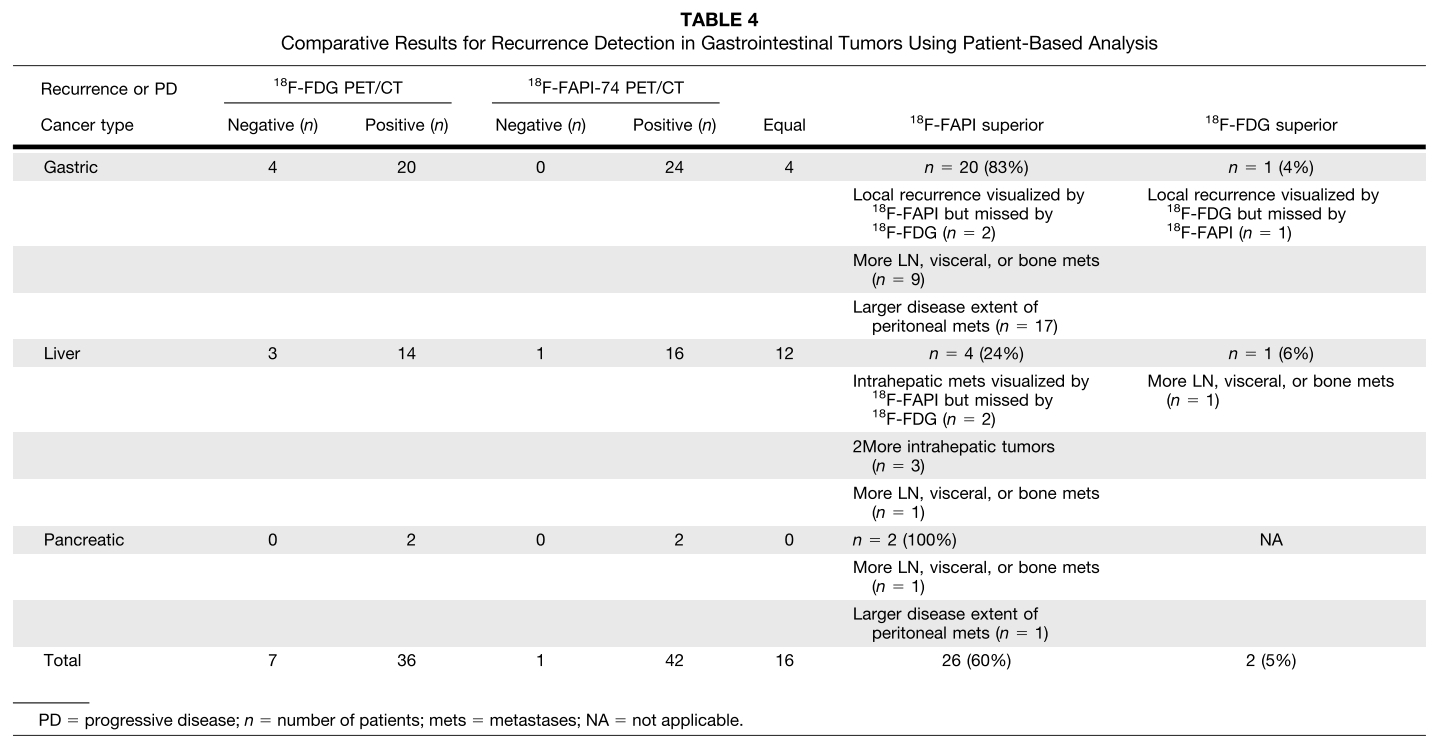
表4. 消化系统肿瘤复发/转移灶的PET/CT对比结果(进展期患者)
研究小结
本项前瞻性临床研究系统比较了18F-FDG和18F-FAPI-74 PET/CT在消化系统肿瘤(包括胃癌、肝脏和胰腺癌)中的诊断效能。研究结果显示:与18F-FDG相比,18F-FAPI-74 PET/CT在消化系统肿瘤原发灶及复发转移灶的诊断方面表现出了更为优越的灵敏度及准确性,大多数的原发肿瘤和转移病灶在18F-FAPI-74 PET/CT中具有更高的显像剂摄取及更好的靶/本底比。然而,在特异性方面,18F-FAPI-74并没有显示出较18F-FDG的明显优势。
此外,与18F-FDG相比,18F-FAPI-74 PET/CT检查无需空腹或血糖水平监测,减少了患者的准备时间,改善了PET/CT的检查流程。此外,在胃肠道中,18F-FAPI-74 PET/CT的生理摄取较18F-FDG更低,改善了PET/CT的图像对比度。因此,除了具有更高的病变检出率,18F-FAPI-74在PET/CT检查及图像采集过程中可能具有更好的临床应用前景。
主要作者介绍
通讯作者

陈皓鋆,厦门大学附属第一医院核医学科副主任医师,副教授,硕士生导师;第21届全国青年岗位能手,入选2023中国研究型医院学会“研究型人才”,福建省卫健委高层次领军人才,厦门市“青年双百人才”;担任欧洲核医学会(EANM)会刊《Eur J Nucl Med Mol Imaging》编委、《中华核医学与分子影像杂志》编委;研究方向为核医学分子影像及核素诊疗一体化,侧重使用Ga-68标记探针进行肿瘤分子成像,使用β射线发射体Lu-177 标记的多肽或小分子进行放射性核素治疗。近5年以通讯/第一作者在权威期刊发表研究论著40余篇,其中14篇发表在《Clin Cancer Res》、《Radiology》、《J Nucl Med》。作为项目负责人主持包括国家自然科学基金、福建省杰出青年科学基金、福建省卫健委重大项目在内的多项科研课题,并作为主要研究者牵头临床研究8项。研究成果在2021-2022连续2次荣获欧洲核医学会“年度最佳论文奖”,北美核医学会(SNMMI)“杰出青年科学家奖”(SNMMI Ones to Watch, TOP 30)、SNMMI青年专家委员会“临床研究奖”第1名;2020年获中华医学会核医学分会“希望之星”奖,并以第一完成人获厦门市科技进步二等奖。
第一作者

徐伟植,厦门大学2021级硕士研究生,曾获厦门大学2022及2023年度“三好学生”、研究生“国家奖学金”等荣誉。以第一或共同第一作者在J Nucl Med、Eur J Nucl Med Mol Imaging、Clin Nucl Med等国际一流期刊发表SCI期刊论文10余篇。

蔡佳宇,厦门大学2022级硕士研究生,曾获厦门大学“三好学生”、研究生“国家奖学金”等荣誉。以第一或共同第一作者在J Nucl Med、Eur J Nucl Med Mol Imaging、Clin Nucl Med等国际一流期刊发表SCI期刊论文10余篇。

彭添兴,高级工程师,福建师范大学硕士研究生,中华医学会核医学分会第十届委员会放药学组委员,福建省医学会核医学分第七、八委员会技术学组委员。2004年至今主要从事放射性药物的合成研究及质量控制工作,作为项目组主要成员,先后参加了多项课题研究,共发表10余篇论文。