近期,厦门大学附属第一医院临床医学研究院宁万山科研团队联合中国医科大学附属盛京医院团队,在国际知名期刊《Circulation-Heart Failure》(中科院一区,IF=8.4)发表了题为“Succinylation of SERCA2a at K352 Promotes Its Ubiquitinoylation and Degradation by Proteasomes in Sepsis-Induced Heart Dysfunction”的重要研究成果。该研究系统阐明了蛋白质琥珀酰化修饰在脓毒症心肌功能障碍(Sepsis-induced Myocardial Dysfunction, SIMD)中的关键作用,创新性揭示了SERCA2a蛋白K352位点琥珀酰化通过促进其泛素化降解导致心肌损伤的分子机制,为脓毒症心肌损伤的临床干预提供了潜在靶点。
研究团队通过高精度质谱技术,在脓毒症大鼠心肌组织中鉴定到10,324个琥珀酰化修饰位点,其中1,042个位点呈现显著差异表达。人工智能驱动的功能预测模型(pFKsucc)结合实验验证,首次发现SERCA2a(心肌肌浆网钙泵)K352位点的琥珀酰化修饰是导致心肌收缩功能障碍的关键分子事件。
研究揭示脓毒症条件下,SERCA2a K352位点的琥珀酰化修饰通过促进K48连接型泛素化链的形成,加速其被蛋白酶体降解(图1)。这一发现首次建立了琥珀酰化修饰与心肌钙循环紊乱的直接联系,为理解脓毒症心肌损伤的分子机制提供了全新视角。
团队发现去乙酰化酶SIRT2可作为SERCA2a的去琥珀酰化酶,通过特异性去除K352位点的琥珀酰化修饰,显著恢复SERCA2a蛋白稳定性。动物实验证实,靶向干预该位点可显著改善脓毒症模型的心肌收缩功能,为临床治疗带来新希望。
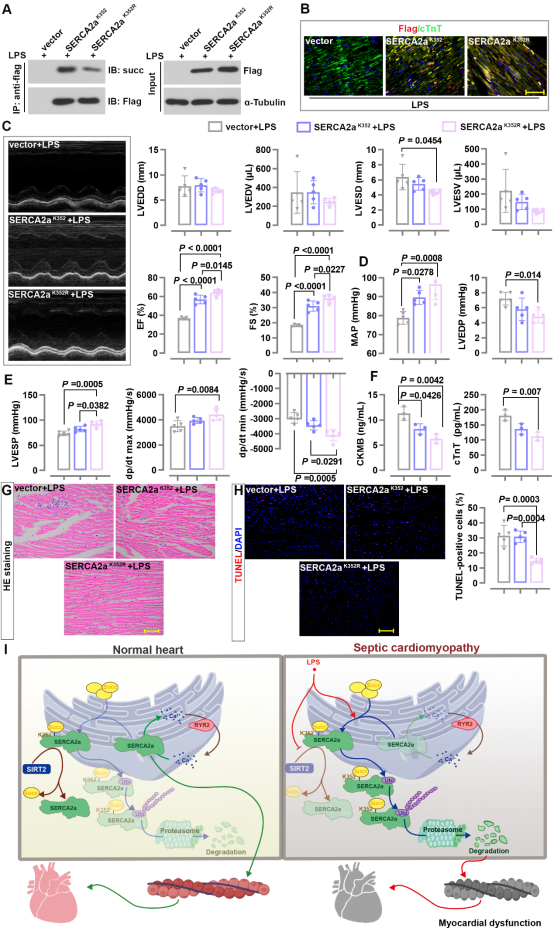
图1. SERCA2a K352琥珀酰化修饰的分子机制与治疗策略
中国医科大学附属盛京医院张铁凝、厦门大学附属第一医院临床医学研究院宁万山为本论文的共同通讯作者。本研究获国家重点研发计划、国家自然科学基金和辽宁省科学技术重大专项等多项项目资助。
宁万山,厦门大学附属第一医院临床医学研究院副研究员,福建省高层次人才、厦门市高层次人才和厦门市“青鹭英才”优培计划引进人才。近年来,以第一/通讯作者身份在Immunity、Nature Biomedical Engineering、National Science Review、Nucleic Acids Research、Circulation Research、Theranostics和Cardiovascular Diabetology等高水平国际期刊发表SCI学术论文21篇,获授权发明专利13项,软件著作权2项。主持国家级项目3项,主持福建省项目1项,参与多项国家科技部重点研发计划项目。